简介
SystImmune公司拥有自己的抗体研发平台,他们的目标是快速构建高产量表达双特异性的抗癌抗体的单克隆细胞系,用于实体瘤的治疗。
SystImmune的细胞系开发
SystImmune 使用CHOZN® (Sigma) 作为表达平台。CHOZN® GS-/- CHO细胞系是一种内源性谷氨酰胺合成酶敲除细胞株,为必需氨基酸谷氨酰胺营养缺陷型,很容易据此来进行筛选。
在此平台上, SystImmune采用微池(minipool)方式来挑选高表达的克隆。但同时这样做会在开始的时候花费较长的时间,最终还是期望得到高表达的细胞系。
除了CHOZN平台和微池挑选法,SystImmune还采用Solentim Cell Metric™成像仪配合有限稀释应用于细胞系开发,这不仅帮助他们解决了单克隆源性的问题,更可以直接生成用于提交IND申请的直接文件证据。
应用以上方法,SystImmune能够从大量的转染微池中成功筛选单克隆细胞系构建研究细胞库(RCB),产品产量至少为1g/L。
细胞系研发过程总览
SystImmune已经开发出一套成熟的细胞系开发流程,过程如图所示。

微池转染和挑选:
CHOZN细胞被转染进感兴趣的基因,每孔铺5000-10000细胞。由于采用了CHOZN系统,回收率很高,例如接种2-5板,回收率可达约80%。到第14天时孔中会有大量多克隆细胞。由于扩增所有微池是很困难的,因此会进行滴度测定来排除不表达的细胞微池。
微池的扩增和筛选:
产物表达最高的50个微池会选来扩增(通过静态培养和摇瓶),筛选并做滴度测定。静态扩增包括将微池细胞从96孔转至24孔板,然后转至T25和T75瓶中培养。摇瓶扩增包括将微池中的细胞扩增,后转至30mL补料分批培养摇瓶中。SystImmune要对30mL补料分批培养产物进行滴度测定,这样做的原因是有时静态扩增的滴度数据同最终生物反应器中滴度数据并不一致。
微池细胞有限稀释:
至少挑选3个微池,用40块96孔板进行有限稀释操作。首先实验用0.3-1个细胞/孔进行铺板,最后选择了最优的0.5个细胞/孔进行铺板。
克隆源性确证和存档:
Solentim Cell Metric imager用于对40块细胞板进行拍照,分别追踪其在Day 0, Day 1 和Day 2的细胞分裂情况,并在Day 7拍照显示其克隆形成情况。在此阶段,SystImmune确认了约200-300个克隆有着高滴度值,但通常选择至少50个Cell Metric确认的滴度最高的单细胞扩增克隆。这种单细胞克隆的确认是非常严格的,并需要生成相关报告用于提交IND。
克隆扩增:
先前步骤中选出的高表达克隆(基于图像和滴度数据)用先前同样的方法,从静态培养到摇瓶培养进行扩增。另用一个30mL摇瓶补料分批培养,将高表达克隆继续扩增。
克隆评价:
SystImmune基于细胞生长和滴度测试来最终确定哪些克隆被送到生产部门,并还需要将细胞培养上清进行纯化交到分析部门,进行蛋白质量检测——CE-SDS(毛细管电泳-SDS聚丙烯酰胺凝胶电泳),HPLC-SEC(高效液相-尺寸排阻色谱),CIEF(等电毛细聚焦),结合和功能测试。他们同样要检测拷贝数,检测支原体。
生产部门:
最终SystImmune挑选了8个产量最高的克隆送去生产部门,进行3L生物反应器发酵,进行活细胞密度(VCD)和IgG产量分析。
产生候选克隆:
最终最好的候选克隆被挑选出来,创建研究细胞库(RCB)。
细胞系开发过程中面临的挑战
同其他公司的CLD部门一样,SystImmune公司在日常工作中也面临着一些关键的问题:
- 细胞系开发过程中多步骤的复杂性
- 部门人手不够
- 降低时间周期及成本
- 每个步骤中形成良好的规则
- 提交IND申请时可以形成规范的文件
- 可以证实细胞的克隆源性
对于后面两点,同其他公司一样,SystImmune公司已经敏锐地觉察到FDA对于细胞系单克隆源性的要求,FDA的Sarah Kennett博士曾做过“Establishing Clonal Cell Lines – A Regulatory Perspective’ presentation”的报告。里面概述了ICH Q5D的条款“For recombinant products, the cell substrate is the transfected cell containing the desired sequences which has been cloned from a single cell progenitor”。
但是,要真正得到单克隆的商用细胞系,以及提供相关证据文件是一件比较困难和繁杂的事情。在过去,许多细胞系开发团体用传统的两轮有限稀释加上理论统计分析证据来实现细胞系开发。但是SystImmune认为这是一种非常繁琐冗杂的步骤,而且最终看到的细胞克隆团并不能证明其来自于一个祖细胞。即便泊松分布被引入用于计算克隆形成的可能性,但实际情况可能受到多种因素的影响,比如宿主细胞的选择,细胞行为,状态,细胞培养环境的改变等。
为细胞的克隆源性存档
SystImmune选择在细胞系的开发过程中使用Solentim的Cell Metric CLD来为细胞的克隆源性存档。Cell Metric可以对细胞孔进行高锐利度的整孔成像,提供Day 0时的细胞状态,从而为单克隆源性提供关键证据,因此只需要一轮克隆即可。
下图展示了SystImmune如何利用Cell Metric来捕获图片,区分单克隆和非单克隆细胞团,从而挑选合适的克隆来进行细胞系开发的过程。

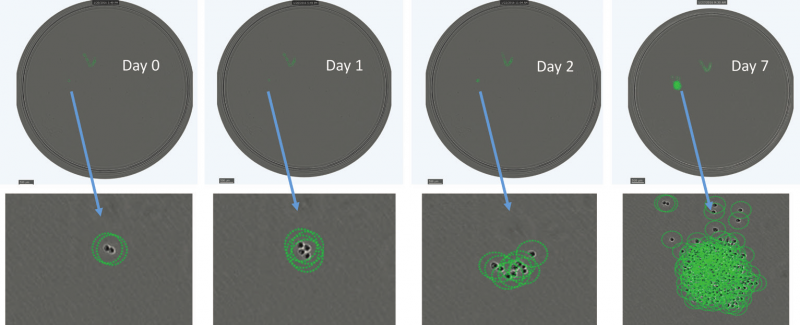
为了提供克隆源性的证据,下图展示了SystImmune利用Cell Metric配套软件的的“输出克隆报告”功能制作的报告文件。报告中展示了对所需要的细胞孔的整孔成像,接种细胞的具体位置,细胞如何随时间逐渐分裂生长为一个克隆团(此处仅显示了Day0和Day1).同样地,孔内同细胞形态相似的一些碎片和杂质也会被拍到。这些碎片或杂质是不会随着时间而发生任何形态上的变化的,这也是证明该克隆团为单克隆的重要基础。

产品检测
如前所述,8个最佳克隆团挑选进入生产部门的生物反应器,进行活细胞密度和IgG产量的检测。
如图所示,7个克隆(1个克隆丢失)经历14天的发酵培养后,活细胞密度和蛋白产量呈现出明显的差异。有3个克隆在第14天测定产品滴度时达到1g/L。有趣的是有一个克隆产量最高,而活细胞密度却最低。因此SystImmune最终选用该细胞来进行后续的研究。

总结
使用CHOZN平台和以前的两轮有限稀释,SystImmune大概要用20周的时间获得一个好的候选细胞系交给生产部门,这是一个非常耗时的过程,对于提交一个IND申请这是一个重要的限速步骤。
阐明细胞的单克隆源性在政策法规层面是非常重要的。SystImmune使用Cell Metric CLD能够很好的捕获细胞接种,数量增长直至形成克隆团的图像。
使用Cell Metric,SystImmune在细胞系建立过程中可以去掉一轮的有限稀释,这意味着可以节省6-8周的时间仍能够达到法规的要求。
本文摘自Solentim 官网,原文链接。
