从2019年开始到2020年,Universal Cells陆续购买了11台Cell Metrics设备。为什么对治疗用细胞产品而言,单克隆性(clonality)如此重要?
“细胞和基因治疗公司正试图采用一种‘可变’的起始材料 – 这是有风险的,而且会使工艺开发复杂化– 而如果使用一种稳定的起始材料,则可为你提供稳定的终产品输出。” 在开发工艺的正确阶段建立高质量的细胞库至关重要。
当决定改进iPSC工作流程时,EverCell选择了Solentim的VIPS™解决方案,该方案提供单细胞克隆,基于图像的克隆性证据和“双重保险”的监管提交。
关键词:干细胞,克隆性,细胞和基因治疗
两年十一台Cell Metric

从2019年开始到2020年,Universal Cells陆续购买了11台Cell Metric成像设备,用于主细胞库单克隆性的确证,而且新型号的设备采购预算仍在编列中。位于美国西雅图的这家“通用型“细胞治疗公司,其创始人CSO是美国基因与细胞治疗学会前任主席,华盛顿大学的David Russell教授,公司2018年被安斯泰来制药(Astellas Pharma)收购。
非常有特点的是,该公司采用一种重组腺相关病毒(rAAV)介导的单链DNA同源重组来“编辑”人基因组序列的技术,而不使用有遗传毒性如Cas9的核酸酶(原理见图一)。与基于核酸酶的基因组编辑不同,该技术不需要DNA链断裂,不产生基因组的脱靶改变,也不产生靶位点上不必要的突变,也不引入外源核酸酶基因。
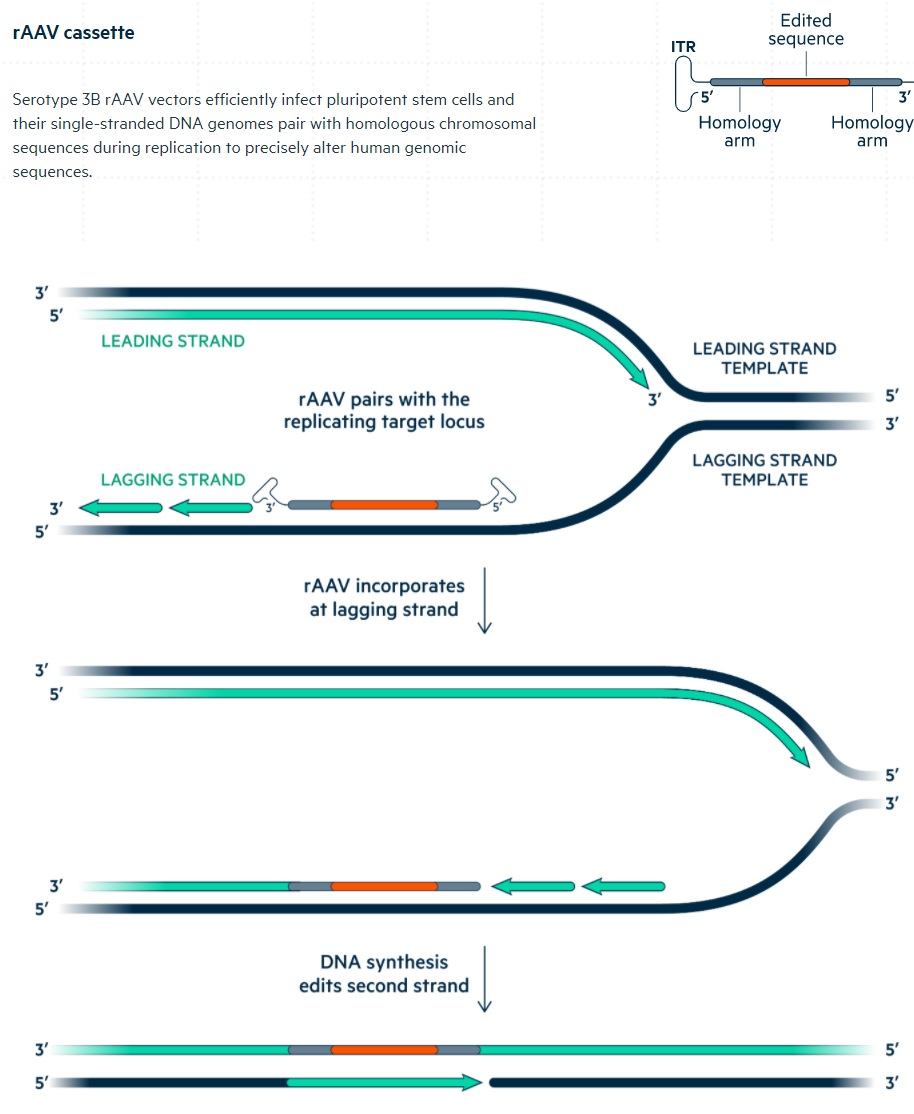
图一:Universal Cells rAAV介导的基因编辑技术原理示意。
Universal Cells通过对人干细胞(ESCs和iPSCs)的临床级基因编辑,生产定制的干细胞,包含在任何基因组位置的缺失、插入或点突变。这些细胞经过编辑、克隆和扩展,形成可以分化成多种治疗产品的主细胞库。例如,通过基因编辑消除多态HLA蛋白的表达,表达特定的非多态HLA分子,提供必要的I类信号,阻止自然杀伤细胞对其裂解,并引入自杀基因以增强安全性等,最终得到“万能”的细胞供体,即适用于每个患者的无免疫排斥的用于移植的万能细胞,这种细胞无需细胞配型和免疫抑制。(1)
2020年1月,Adaptimmune和Universal Cells签署了进一步的共同开发和商业化协议,将为癌症患者提供三种新的干细胞衍生的异体T细胞疗法。Adaptimmune和UniversalCells的科学家已经合作编辑掉HiPSCs中可能被免疫系统识别的元件,用以生产“通用型“或称为”现货“(off-the-shelf)的供体T细胞,这些异体产品有望大批量生产相同的T细胞来治疗大量的患者。(2)
为什么对治疗用细胞产品而言,单克隆性(Clonality)如此重要?
细胞和基因疗法有可能会彻底改变医学,让医生治愈以前无法治愈的疾病。但是,开发一个可生产,稳定且一致的产品的工艺是一个不小的技术挑战。
同样位于美国西雅图的CDMO Pluristyx公司的联合创始人Benjamin Fryer说,一个主要的挑战是,需要小心处理原始材料,即用于生产药物的细胞。他说:“如果能处理好第一步,就能降低整个工艺的风险,并有可能创造治愈疾病的治疗方式。”
“细胞和基因治疗公司正试图采用一种‘可变’的起始材料 – 这是有风险的,而且会使工艺开发复杂化– 而如果使用一种稳定的起始材料,则可为你提供稳定的终产品输出。” Fryer在“细胞和基因治疗生物工艺和商业化在线会议”上告诉与会代表,在开发工艺的正确阶段建立高质量的细胞库至关重要。(3)
Fryer表示,部分挑战在于,在科研实验室进行“建库”的方法往往更类似于一种“进行中”的培养过程,而不是开发一个明确的、稳定细胞库。“在研发实验室,你从你的原始物料开始工作 – 也许是人胚胎干细胞系,也许是来自患者的供体细胞系 – 细胞可能被传代,并在实验室中共享。当有人需要一些细胞时,他们只需从正在进行的培养工艺中提取即可。”
“但当你试图将这一研究过程转化为临床级生产时,你必须将其分解成独立的单元操作,且需要受到严格的监管。”
Fryer说,第一步应该建立一个临床级的冻存细胞库,从中可以生产有效的细胞库和种子库。“真的,如果你要遵循这种单元操作系统,前三个单元 – 种子库、扩增和主细胞库,以及潜在的基因修饰– 必须完成,这样它才能在产品的整个生命周期中确保工艺供应。”
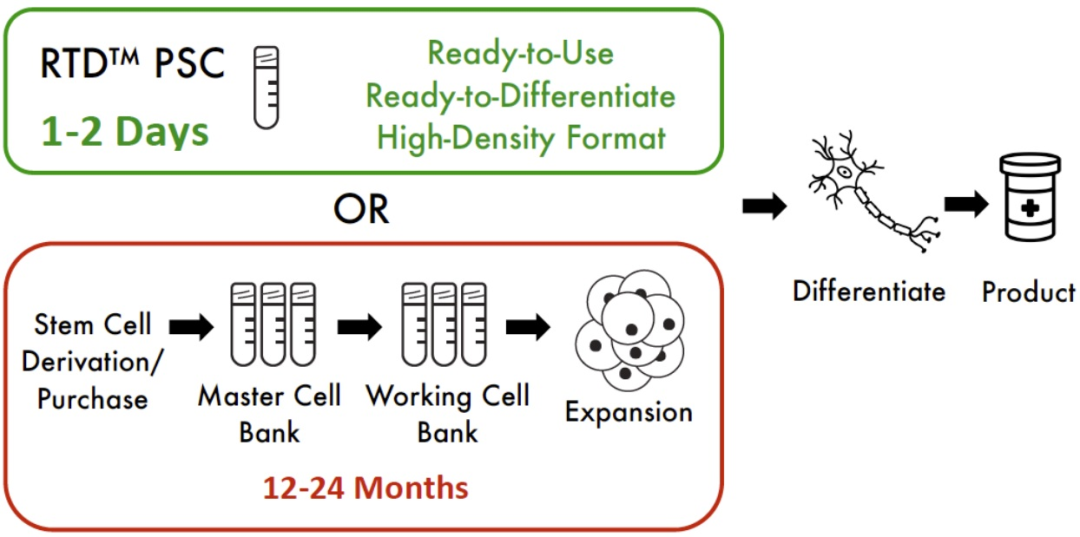
图二:Pluristyx公司提供的服务示意。
建立hiPSC用于细胞治疗的新工作流程
当对“敏感又善变”的人干细胞进行单克隆时,现有的工作流程和方法确很难实现单克隆性的确证和符合相关监管的要求。比如预先包被的基质会影响成像的清晰度,而且有动物成分,此外大量的手工操作步骤很难建立起标准化的工作流程。
EverCell Bio是美国麻州一家为干细胞技术应用于细胞治疗提供定制服务的供应商,专长于人源细胞建模,如供体细胞系的建立、重编程、基因编辑和分化。当决定改进iPSC的工作流程时,EverCell选择了Solentim的VIPS™解决方案,该方案提供单细胞克隆,基于图像的克隆证据和“双重保险”的监管提交。(4)
当问起hiPSC应用于细胞治疗领域有哪些挑战时,该公司创始人和总裁Philip D. Manos说:“有很多!其中有两个关键的挑战,一是hiPSCs的敏感性,需要专门的培养基和基质,并且单个hiPSC细胞在没有ROCK-inhibition时存活/附着较差。目前hiPSC都是用一小团细胞去传代,并不是对单个细胞培养来增殖,这对需要进行单细胞操作的体外策略如基因编辑制造了障碍。第二,hiPSCs 具有内在的可变性(inherently variable),这意味着与干细胞打交道的流程需要尽可能地标准化,来确保得到有意义的数据。然而,目前的培养方法几乎完全是人工操作的,难以避免人为的错误,因此标准化工作流程是个重大的技术挑战。”
VIPS组合使用MatriClone基质建立的新工作流程让Manos非常满意。“当谈到单细胞验证和随后的克隆性监管报告时,VIPS似乎是独一无二的,遥遥领先。“,”我也很满意Solentim提供的双保险确证,通过将入孔单细胞验证成像与第0天的生长和克隆特性成像相结合来实现。这在克隆报告中都有记录,便于查看和分享。”

Philip Manos, President at EverCell
此外,针对之前所提的两个主要挑战,Matriclone无动物来源成分,无需预先包被,可以和细胞混合在一起做单细胞铺板,与VIPS结合使用建立的标准工作流程,可以轻松实现同时开发多个iPSC细胞株,让EverCell Bio的研发流程时间缩短了近一半,在20天内就可以建好一个细胞库。
“我们预见VIPS系统将帮助我们在基因编辑相关的项目中提高速度、质量和克隆性的可信度”,Philip D. Manos总结说。
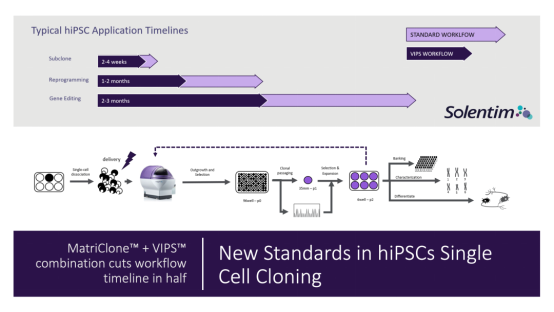
图 三: Solentim新技术加速hiPSCs细胞株开发流程。(请点击图片横屏放大浏览)
